ISO15189认证流程
医学实验室ISO15189 认可流程
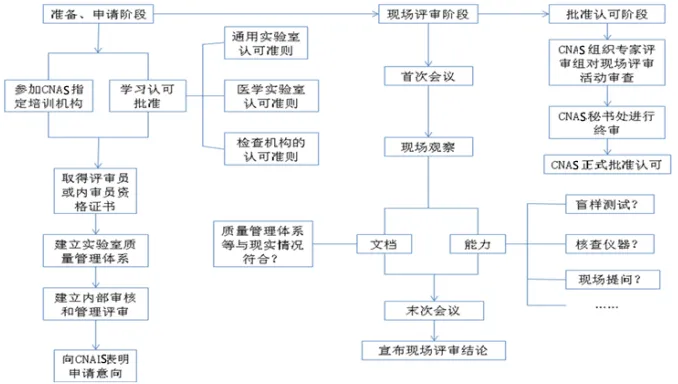
医学实验室认可过程
1、准备及申请阶段
(1)准备
实验室认可完全是各实验室自己的自觉自愿行为。实验室可根据自身现实情况和发展需要自行决定是否参加认可
(2)申请应满足的条件一般包括
申请方具有明确的法律地位,可依法从事所申请认可范围内的相关活动;
按CNAS-CL02《医学实验室质量和能力认可准则》及相关政策建立质量管理体系并至少运行六个月;
至少进行一次完整的管理评审和内部审核;
有能力从事所申请认可范围内的相关活动;
截止至申请日的一年内至少参加过两次CNAS承认的能力验证活动或实验室间比对,且对不满意结果已进行了有效整改;
具备3个月内接受现场评审的条件;
按要求提交全部认可申请相关的资料并缴纳费用。
2、现场评审阶段
预备会:评审组长在现场评审前负责召开有全体评审组成员参加的预备会;
首次会:评审组长主持召开由评审组和实验室有关人员参加的首次会议;
现场评审:根据《现场评审日程表》进行,并对评审过程予以记录;
座谈会:初次评审和复评审时,现场评审期间应召开一次医护人员座谈会;
评审组内部会:在现场评审期间,评审组长应每天安排一段时间召开评审组内部会;
与实验室沟通:评审组在每天工作结束前,应与实验室代表简要沟通当天的评审情况;
末次会:评审组根据现场收集的客观证据对实验室的质量管理体系运行情况和技术能力进行客观分析,综合评价;
后续工作:评审组离开现场前,应封存现场试验报告及原始记录,连同评审报告、附表和相应附件的复印件,留存实验室;
跟踪验证:现场评审后,评审组长或其指定的评审员应在规定时限内对实验室的纠正措施进行跟踪验证和确认。
3、批准认可阶段
CNAS组织专家评审组对所有资料进行程序性和规范性审查;
CNAS秘书处对专家评审组的报告及相关资料,进行最终审查;
CNAS向实验室提出整改要求,整改满意后;
CNAS正式批准认可,被认可的单位即可使用实验室认可的标志。
iso15198认可准则
中国合格评定国家认可委员会(CNAS)秘书处已完成CNAS-CL02:2012《医学实验室质量和能力认可准则》(等同采用ISO 15189:2012)的修订换版工作。CNAS-CL02:2023《医学实验室质量和能力认可准则》(等同采用ISO 15189:2022)于2023年6月1日发布,2023年12月1日实施。
中国合格评定国家认可委员会 (CNAS)秘书处已完成CNAS-CL02-A001:2023《医学实验室质量和能力认可准则的应用要求》和CNAS-EL-14:2023《医学实验室认可受理要求的说明》的修订工作,相关文件于2023年8月1日发布,于2023年12月1日实施。
ISO 15198是一项针对医疗实验室的质量管理体系标准,也称为“医疗实验室质量管理体系要求和评价指南”。该标准旨在帮助医疗实验室确保其测试结果的准确性和可靠性,以及提供高质量的医疗服务。
ISO 15198标准要求医疗实验室建立和实施质量管理体系,包括质量策略、质量手册、程序文件、记录和文件等,以确保实验室的测试过程符合标准和法规要求,并满足顾客需求和期望。该标准要求实验室进行内部审核和管理评审,以及接受外部审核和评估,以确保质量管理体系的有效性和持续改进。
ISO 15198标准还要求医疗实验室建立和实施质量控制措施,包括校准、质量控制、质量保证和质量改进等,以确保测试结果的准确性和可靠性。该标准还要求实验室进行风险评估和管理,以确保测试过程的安全和可靠性。
ISO 15198标准适用于各类医疗实验室,包括临床化验室、病理学实验室、微生物学实验室等。建立和实施ISO 15198质量管理体系需要全员参与和持续改进,以确保医疗实验室的测试结果的准确性和可靠性,提高医疗服务的质量。




